マルホは、有効成分の効果を最大限に引き出し、副作用を最小限に抑えた、誰もが使いやすい医薬品の開発を目指しています。そのような医薬品を患者さんにいち早く届けるために、デジタル技術を使った最新の医薬品開発に取り組んでいます。
近年、スマートフォンやクラウドコンピューティング、AIなどのデジタル技術によって私たちの⽣活は⼤きく変わってきましたが、医薬品開発も⼤きな影響を受けています。標的分⼦の特定、有効成分の創出のほか、有効成分の有効性∕副作⽤の発現をコントロールし、安定性や利便性を最適化する「製剤設計」に対するデジタル技術の適⽤が注⽬されています。
製剤設計では、1,000種類以上の医薬品の添加物と有効成分の組み合わせから、⽬標とする医薬品の性能を満たす最適な条件を⾒つける必要があります。マルホは製剤設計に確かな強みを持っており、これまでに蓄積した知⾒や技術に加えて、デジタル技術を活⽤することで、製剤設計を効率化‧⾼質化する取り組みを始めています。 例えば、社内や世界のデータを利⽤して最適な条件を計算できる⼈⼯知能や、化学物質間の相互作⽤と製剤の特性を計算できる分⼦シミュレーションなどに挑戦しています。
▲デジタル技術と製品創出の関係
今回は、デジタル技術を駆使する最先端の研究「デジタル製剤学」について、マルホの挑戦をご紹介します。
機械学習と呼ばれる、まるで⼈間のように学習したコンピュータが、データに潜む特定のパターンを⾒つける技術を⽤いて、効率的に製剤を開発することをめざしています。機械学習が発達すれば、何パターンもの添加物の組み合わせを⾼精度かつ⾼速に予測することができ、製剤開発にかかるコストを⼤きく減らすことができるようになります。
マルホでは、外⽤剤の開発において、有効成分の経⽪吸収性(有効成分が⽪膚からどれだけ吸収されるか)を予測するAIを構築してきました1-3)。外⽤剤の有効性や安全性評価の観点から、経⽪吸収性は外⽤剤開発において重要視される指標の1つです。412種類の製剤パターンのデータを⽤いて構築したAI は、外⽤剤の経⽪吸収性を正確に予測できることが⽰されました2)。
さらに、構築したAIを発展させて、有効成分の溶解性や安定性も含めて、外用剤を開発する際の条件を提案するシステムを作り、実運用できるようにしています4)。このシステムはコンピュータ上のみで完全に動くため、低コスト・超高速であることはもちろん、生物から得られる材料を使う必要もなくなります。医薬品の有効成分が手元にないときにも、製剤開発の可能性を探ることができるようになり、極めて効率的に医薬品を開発できる可能性を秘めています。
AIは強⼒な製剤設計の⽀援ツールとなり得ますが、学習させるデータを事前に揃える必要があるというデメリットもあります。多様な製剤の幅広い特性を収集しようとすると、膨⼤なコストがかかってしまうことも。⼀⽅、医薬品製剤が分⼦によって構成されていることから考えると、分⼦同⼠に働く⼒から各分⼦の動きを予測する「分⼦シミュレーション」技術によって、⼤量のデータを必要とすることなく、複雑な製剤の特性を予測できるかもしれません。マルホでも、分⼦シミュレーションを利⽤した製剤特性の予測に関する検討を進めています。
様々な液体における有効成分の動き5)や、各成分がきれいに混ざるかなどを精度よく予測できることを確認しており、医薬品の添加物の影響を含めたdrug deliveryの解析に対して「分⼦シミュレーション」が役⽴てられると期待しています。マルホでは、AIや分⼦シミュレーション研究に向けて、社内の計算資源の整備や、社外のスパコンを含めた計算資源の活⽤など、そのバランスや運⽤⽅法の最適化を進めています。
デジタル技術は驚くべき速さで日々進歩しています。将来的には、独自の新しいアイデアをコンピュータ上でバーチャルに評価することができるようになると考えています。また、世界中の情報を学習し、かつ分子シミュレーションとも連携したAIが、製剤課題の解決法やエビデンスを提示してくれる、研究者の最も身近なパートナーとなるかもしれません。
マルホはそのような未来に向けて、社内の研究を進展させるだけに留まりません。従業員による、デジタル製剤学に関連した学会のフォーカスグループの執行部としての運営、各種シンポジウムのオーガナイズ、関連学会等での招待講演や論⽂公表、他社との意⾒交換などの社外活動などの支援も行っています。
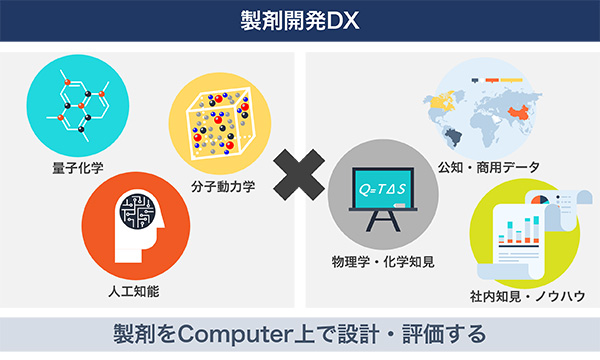
▲世界中の情報を学習したAI(外用製剤設計用のデジタルプラットフォーム)の開発を目指しています
新しい医薬品開発のあり⽅を⽣み出したいというワクワクを胸に、ミッション「あなたといういのちに、もっと笑顔を。」もたらせるよう、マルホはデジタル製剤学にますます取り組んでいきます。
【出典】
1)Baba H. et al.:Pharm Res. 2015; 32, 2360-2371.
2)Baba H. et al.:Pharm Res. 2015; 32, 3604-3617.
3)Baba H. et al.:Int J Pharm. 2017; 522(1-2), 222-233.
4)馬場廣海:ファルマシア. 2024; 60(2), 116-121.
5)Baba H. et al.:J Comput Chem. 2022; 43(28), 1892-1900.
