皮膚外用薬のレシピの特徴 レシピの特徴2:基剤・製造方法が皮膚外用薬に与える影響
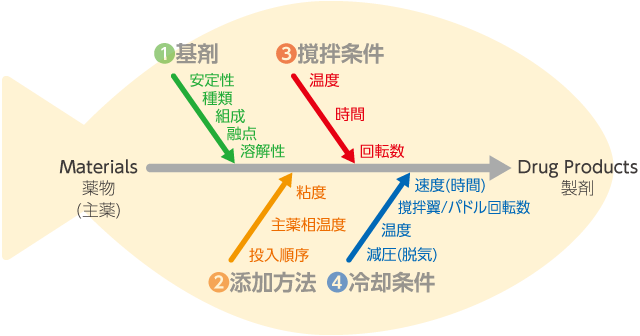
皮膚外用薬が薬物(主薬)から製剤として完成する過程では、①基剤や、製造方法の条件である②添加方法、③撹拌条件、④冷却条件などが製剤の特性(性質、性状など)や品質を決定する主な要因として挙げられます(図1)。皮膚外用薬は、主薬に合った基剤や製造方法を選択し、有効性、安全性、品質および使用感を考慮した最適な製剤として設計されています。そのため、皮膚外用薬は、主薬が同じであっても基剤や製造方法が同じでないと、異なる特性や品質を示し1)、主薬の放出性や経皮吸収性に影響を及ぼすことが報告されています2)。
今回は、クリーム剤の処方を中心に説明します。クリーム剤は、水性成分と油性成分が基剤中に乳化しており、水中油型(O/W)と油中水型(W/O)の2つに大別されます(図2)。O/Wでは水性成分の中に油滴が均一に分散しており、W/Oでは油性成分の中に水滴が均一に分散しています。しかしながら、水性成分と油性成分はそのままでは分散しません。これら2つを均一に分散させるために、乳化を目的とした添加物である界面活性剤を用い、安定な乳化物として製剤化していきます(図2)。クリーム剤の一般的な製造方法では、油相と水相のいずれかの相に主薬を加えて、それぞれを加温し、油相および水相を合わせて全体が均一になるまでかき混ぜる乳化工程が必要となります。
このような方法でクリーム剤は製剤化されますが、基剤や製造方法の違いが、W/Oクリーム剤の品質、配合安定性および皮膚生理機能に与える影響を具体的に紹介します。
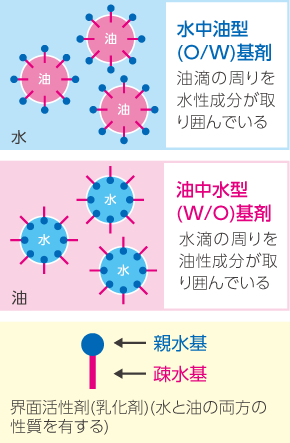
界面活性剤は図2の3つ目のように水になじみやすい親水基と油になじみやすい疎水基を有しており、水性成分と油性成分を橋渡しする機能があります。これにより、O/Wでは外側の水性成分に親水基、内側の油性成分に疎水基を配列することで油滴を水性成分に分散させることができ、見かけ上、混じり合った状態を作ります。W/Oでは逆に配列します。
1.基剤や製造方法を変更した場合の製剤の品質への影響3)
1-1 基剤を変更した場合
皮膚外用薬において、基剤の選択は重要です。同じ成分であっても、基剤のメーカーやグレードの違いによって製剤の品質に違いが生じることがあります。例えば、メーカーの違いによって融点や硬さなどが異なります。同一メーカーであっても、グレードの違いによっても同様に異なります。グレードの違いとは、品質の良し悪しではなく、性状(固形・液体)、融点や精製度(純度)などが異なることを指します。皮膚外用薬を設計する上では、最適な基剤を選択し、有効性、安全性、品質および使用感を担保する必要があります。
クリーム剤中に分散する滴のことを乳化粒子といい、一般的に、この乳化粒子径(大きさ)は、小さく均一であると良いといわれ、主薬の均一性、乳化安定性や使用感などに影響を与えます。
ここでは、W/Oクリーム剤から基剤成分の削除、メーカーやグレード変更を行うことで乳化安定性、すなわち、乳化粒子径や製剤の分離状態にどのような影響があるかを評価しました。
W/Oクリーム剤(標準製剤)ならびに基剤を変更した製剤を50℃*1で2週間保管した際の、品質の評価を表1に示します。基剤を変更した製剤の多くが、開始時より乳化粒子径が大きくなり、製剤の分離が認められたことから、基剤の違いが乳化安定性に影響することが分かりました。
*1:短期間で製剤の品質の差を確認するため、加速試験(40℃/75%RH)より過酷な条件の50℃で実施した。
表1:基剤を変更した場合の品質評価
| 製剤名 | 標準製剤 | 油性成分A 削除製剤 |
油性成分B グレード変更 製剤 |
油性成分B メーカー変更 製剤 |
界面活性剤 グレード変更 製剤① |
界面活性剤 グレード変更 製剤② |
||
|---|---|---|---|---|---|---|---|---|
| 乳化安定性 | 乳化粒子径*2 | 開始時 | A | A | A | A | A | A |
| 50℃、2週間保管後 | A | A | C | D | C | D | ||
| 製剤の分離*3 | 開始時 | なし | なし | なし | なし | なし | なし | |
| 50℃、2週間保管後 | なし | あり | あり | あり | あり | あり | ||
*2:乳化粒子径の評価
製剤の顕微鏡観察を行い、乳化粒子径の大きさを測定した。
A:1μm未満の乳化粒子のみ
B:1μm未満~2μmの乳化粒子が混在
C:1μm未満~数μmの乳化粒子が混在
D:1μm~数μmの乳化粒子が混在
*3:製剤の分離の評価
製剤をスピッツ管に充てんし、50℃の恒温器で保管した。所定の期間保管した後、当該サンプルを恒温器から取り出し、遠心した後、製剤の状態を目視にて確認した。製剤上部に分離相が1mm以上確認された場合、分離ありと評価した。
1-2 製造方法を変更した場合
皮膚外用薬においては、製造方法も重要です。同じ基剤を用いても、添加方法、撹拌条件、冷却条件などの製造方法が変わると製剤は異なった品質を示すことがあります。
そこで、標準製剤ならびに同製剤の製造方法を変更した製剤を50℃で2週間保管した際の、品質を評価しました。その結果、製造方法を変更した製剤は、開始時より乳化粒子径が大きくなり、製剤の分離が認められました(表2)。特に、標準製剤と撹拌条件変更製剤①を比較すると、開始時から乳化粒子径に大きな差が認められました(図3)。
このように、基剤同様、製造方法の違いが乳化安定性に影響することが示されました。
表2:製造方法を変更した場合の品質評価
| 製剤名 | 標準製剤 | 添加方法 変更製剤① |
撹拌条件 変更製剤① |
撹拌条件 変更製剤② |
冷却条件 変更製剤 |
||
|---|---|---|---|---|---|---|---|
| 乳化安定性 | 乳化粒子径*2 | 開始時 | A | A | C | A | A |
| 50℃、2週間保管後 | A | B | D | B | B | ||
| 製剤の分離*3 | 開始時 | なし | なし | なし | なし | なし | |
| 50℃、2週間保管後 | なし | あり | あり | あり | あり | ||
| 変更内容 | - | 乳化温度を低くした条件に変更 | 手撹拌に変更 | 撹拌回転数は、②>標準製剤>① 撹拌時間は、標準製剤>②>①の条件に変更 | 冷却温度を低く、冷却時間を短縮した条件に変更 | ||
図3:撹拌条件の違いによる乳化粒子径の違い(開始時)

標準製剤
乳化条件を最適化することで、乳化粒子が小さく均一である

撹拌条件変更製剤①
大きな球状の乳化粒子や不溶解物が多く、形や大きさが不均一である
皮膚外用薬の製造には、Fish bone 特性要因図(図1)に示したような①基剤や、製造方法の条件である②添加方法、③撹拌条件、④冷却条件などがあり、基剤や製造方法の違いが製剤の品質を決定する上で重要な要因であることが分かりました。
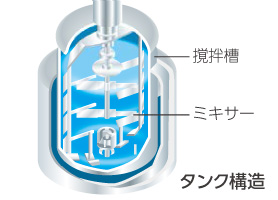
コラム:クリーム剤はどうやって乳化させるの?
クリーム剤は製造する工程で乳化機(図4)を用います。乳化機を用いることで、基剤を均一に混ぜ合わせて乳化させます。その際、基剤の温度、乳化機に基剤を添加する時の投入順序、撹拌時の回転時間・回転数、冷却時の温度・時間など、様々な製造条件があります。クリーム剤を始めとした皮膚外用薬は、有効性、安全性、品質および使用感を最適化するための条件を設定し、製剤設計されています。
2.配合安定性への影響4)
外用療法では、患者さんのアドヒアランスの向上を目的として、皮膚外用薬を混合して処方されることがあります。しかしながら、皮膚外用薬は混合することを目的として開発されていないため、他剤を混合することによって主薬の安定性だけでなく、製剤の特性が変化する可能性があります。また、医療現場では混合によってブリーディング注1)や分離を生じた報告5)もあり、混合時の組み合わせや製剤の特性変化には十分に注意する必要があります。
注1)ブリーディング:成分の融点の違いなどにより、低融点の水・油などの液状成分がにじみ出る現象。
前述した通り、W/Oクリーム剤の基剤や製造方法を変更することで、製剤の品質に影響することが分かりましたが、それらの製剤とステロイド外用薬を混合した場合に、製剤の配合安定性(混和性、ブリーディングおよび乳化安定性)にどのような影響があるかについても評価しました。
方法
標準製剤または表1・2で用いた基剤や製造方法を変更した製剤の一部(表3)とアンテベート軟膏0.05%(以下、A軟膏)またはロコイド軟膏0.1%(以下、L軟膏)を、1:1の割合でビーカーおよび撹拌棒を用いて、3分間混合し、混和性*4を評価しました。混合した配合製剤は暗所保存(25℃/60%RH)し、開始時、1、2、4、8週目のブリーディング*5、乳化安定性*6を評価しました。
*4:混合した際の製剤の状態について「軟化、硬化、水または油の分離」の3項目を確認した。
*5:容器内に充てんした試料に対し、目視によりブリーディングの有無を確認した。
*6:製剤をスピッツ管に充てんし、遠心後に、目視により分離の有無を確認した。
| 変更内容 | 製剤名 |
|---|---|
| - | W/Oクリーム剤(標準製剤) |
| 基剤の変更 | 油性成分A削除製剤、油性成分Bグレード変更製剤、油性成分Bメーカー変更製剤、界面活性剤グレード変更製剤①、界面活性剤グレード変更製剤② |
| 製造方法の変更 | 撹拌条件変更製剤①、撹拌条件変更製剤②、冷却条件変更製剤 |
結果
配合安定性は、標準製剤または基剤や製造方法を変更した製剤の一部とA軟膏またはL軟膏の配合製剤で、問題は認められませんでした(表4・5)。
ブリーディングは、界面活性剤グレード変更製剤②とA軟膏の配合製剤で混合直後から生じ(表4・図5)、図5に示すように水性成分と油性成分の分離が生じました。基剤や製造方法を変更した製剤とL軟膏の配合製剤の一部においては、8週目にブリーディングが認められています(表5)。乳化安定性は、配合製剤の中で唯一、界面活性剤グレード変更製剤②とA軟膏の配合製剤で分離が確認されました(図6)。
このように皮膚外用薬は同じ剤形であっても、基剤や製造方法の違いにより、配合安定性が異なる場合もあるため、製剤の特性変化などに注意が必要になります。
図5:ブリーディング(開始時)(混合後、瓶に移し替えた状況)

- 左:界面活性剤グレード変更製剤②とA軟膏の配合製剤
- 右:標準製剤とA軟膏の配合製剤
図6:乳化安定性(開始時)

- 左:界面活性剤グレード変更製剤②とA軟膏の配合製剤
- 右:標準製剤とA軟膏の配合製剤
| 配合製剤 | 混和性 | 水または油の分離 |
|---|---|---|
| 界面活性剤グレード変更製剤②/A軟膏 | 軟化、液状化 | あり |
| 冷却条件変更製剤/L軟膏 | やや軟化 | なし |
| 上記以外の配合製剤 | 問題なし | なし |
表5:配合製剤のブリーディング
| 変更内容 | 製剤名 | A軟膏と混合時のブリーディング | L軟膏と混合時のブリーディング | ||||
|---|---|---|---|---|---|---|---|
| 開始時 | 1、2、4週間 | 8週間 | 開始時 | 1、2、4週間 | 8週間 | ||
| - | 標準製剤 | ◯ | ◯ | ◯ | ◯ | ◯ | ◯ |
| 基剤の変更 | 油性成分A削除製剤 | ◯ | ◯ | ◯ | ◯ | ◯ | ◯ |
| 油性成分Bグレード変更製剤 | ◯ | ◯ | ◯ | ◯ | ◯ | ◯ | |
| 油性成分Bメーカー変更製剤 | ◯ | ◯ | ◯ | ◯ | ◯ | × | |
| 界面活性剤グレード変更製剤① | ◯ | ◯ | ◯ | ◯ | ◯ | × | |
| 界面活性剤グレード変更製剤② | × | × | × | ◯ | ◯ | ◯ | |
| 製造方法の変更 | 撹拌条件変更製剤① | ◯ | ◯ | ◯ | ◯ | ◯ | × |
| 撹拌条件変更製剤② | ◯ | ◯ | ◯ | ◯ | ◯ | ◯ | |
| 冷却条件変更製剤 | ◯ | ◯ | ◯ | ◯ | ◯ | × | |
ブリーディングなし:○、ブリーディングあり:×
3.皮膚生理機能に及ぼす影響6)
皮膚疾患の治療には、皮膚の生理機能の把握が重要です。皮膚の最外層である角層は、角層の内側の水分の蒸散を防ぎ、外界からの異物(アレルゲン・細菌など)の侵入を防御する役割を担っています。皮膚の生理機能を表す指標として、経表皮水分蒸散量(TEWL)*7と角層水分量があります。TEWLは皮膚バリア機能の評価に、角層水分量は角層の水和状態を表し保湿作用の評価として用いられています。アトピー性皮膚炎などの患者さんは皮膚バリア機能が低下し、皮膚が乾燥しているため、TEWLは上昇し、角層水分量は低下しています。
今回、W/Oクリーム剤の基剤や製造方法を変更することで、製剤の品質や配合安定性に影響することが分かりました。次に、基剤を変更した製剤および基剤と製造方法を変更した製剤を塗布した際、皮膚生理機能(角層水分量および皮膚バリア機能)にどの程度影響を及ぼしているのか、モルモットを用いて評価しました。
*7:経表皮水分蒸散量(Transepidermal water loss:TEWL): 皮膚から蒸散する水分量であり、皮膚バリア機能の指標である。TEWLが高いほど皮膚バリア機能が低下していると考えられる。
方法
雌性モルモット(Slc:Hartley、4週齢)の除毛した腹部皮膚にアセトン(A)およびジエチルエーテル(E)を1:1で混合した溶液および水(W)で処置(以下、A/E/W処置)し、角層水分量を1/3~1/2に低下させ、TEWLを2~3倍に上昇させたモデル動物(ドライスキンモデル)を作製しました。その腹部皮膚に各製剤(表6)を塗布しました(各製剤:n=8)。A/E/W処置前(開始前)、塗布前(0時間)、塗布後3、6、9および24時間後の角層水分量およびTEWLを測定しました。
| 変更内容 | 製剤名 |
|---|---|
| - | W/Oクリーム剤(標準製剤) |
| 基剤の変更 | 油性成分Bグレード変更製剤 |
| 基剤・製造方法の変更 | 組み合わせ製剤(油性成分Aの削除、油性成分Bのメーカー変更、界面活性剤のグレード変更②、添加方法変更②*8、撹拌条件変更①、冷却条件変更) |
*8:水相と油相の投入順序を変更
結果
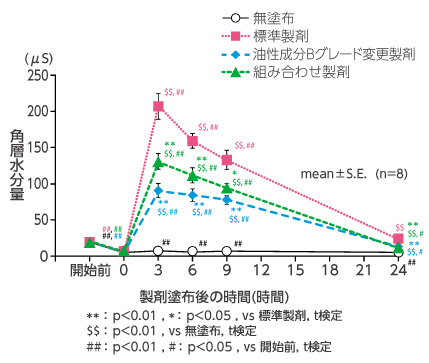
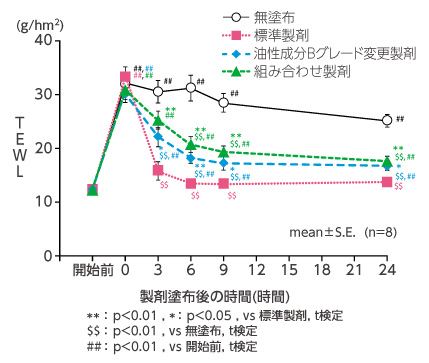
角層水分量は、無塗布部位と比較し、各製剤では塗布後3時間より有意に増加しました(図7)。TEWLは、無塗布部位と比較し、標準製剤および油性成分Bグレード変更製剤塗布後3時間、組み合わせ製剤塗布後6時間後より有意に低下しました(図8)。
製剤塗布後3時間から24時間までの各測定時点において、油性成分Bグレード変更製剤および組み合わせ製剤塗布部位の角層水分量は標準製剤塗布部位に対して有意な低値を示し、TEWLは有意な高値を示しました。
基剤や製造方法を変更することにより、製剤の特性変化などが起こり、皮膚生理機能に影響を与えたと考えられます。
最後に
今回はW/Oクリーム剤を例に挙げ、基剤や製造方法が皮膚外用薬に与える影響についての検討結果を紹介しました。基剤のメーカー・グレードの違い、および製造方法の変更は、品質に影響するばかりではなく、製剤の特性などが変化することで、配合安定性や皮膚生理機能にも影響することが分かりました。
皮膚外用薬は、主薬に合った基剤や添加物、製造方法を選択し、有効性、安全性、品質および使用感を考慮した最適な製剤として設計されています。このように最適化された皮膚外用薬の処方(レシピ)における基剤や製造方法を理解することは、適正使用の推進や患者さんへの服薬説明に役立ちます。
- 出典:
-
- Ashizuka Y et al.:YAKUGAKU ZASSHI 136(8),1161-1169,2016
- Kitagawa S et al.:Chem Pharm Bull 63(1),43-48,2015
- マルホ株式会社社内資料:W/Oクリーム剤を用いた基剤成分の配合意義及び製造方法の重要性に関する検討試験
- マルホ株式会社社内資料:W/Oクリーム剤の基剤及び製造方法変更品を用いた配合変化試験
- 江藤隆史:臨床皮膚科 55(5),96-101,2001
- マルホ株式会社社内資料:W/Oクリーム剤の基剤及び製造方法変更した製剤のモルモットを用いた皮膚生理学的機能に関する検討試験
- 皮膚外用薬のレシピの特徴 レシピの特徴2
-
- 基剤・製造方法が皮膚外用薬に与える影響



