ゼビアックスの感受性データ
尋常性痤瘡患者由来cutibacterium acnes およびstaphylococciに対するオゼノキサシンの抗菌力
cutibacterium acnes およびstaphylococciの臨床分離株に対する抗菌力(in vitro )
2012~2013年に尋常性痤瘡患者より分離されたcutibacterium acnes ※1およびstaphylococci※2に対する各種抗菌薬の最小発育阻止濃度(MIC)をCLSI※3に準じた微量液体希釈法により測定した。
- cutibacterium acnes (C. acnes ) 266株
- Staphylococcus aureus (S. aureus ) 23株、Staphylococcus epidermidis (S. epidermidis ) 229株、Other coagulase-negative staphylococci (Other CNS) 82株
- Clinical and Laboratory Standards Institute
- 濃度測定範囲
- オゼノキサシン:0.06 ~ 16μg/mL
- ナジフロキサシン・クリンダマイシン:0.06 ~ 128μg/mL
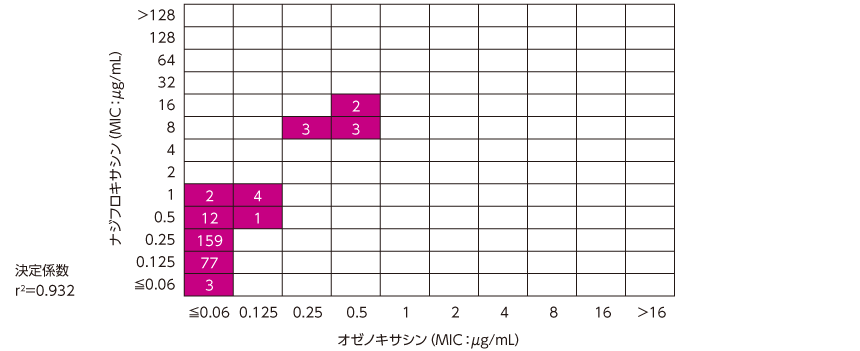
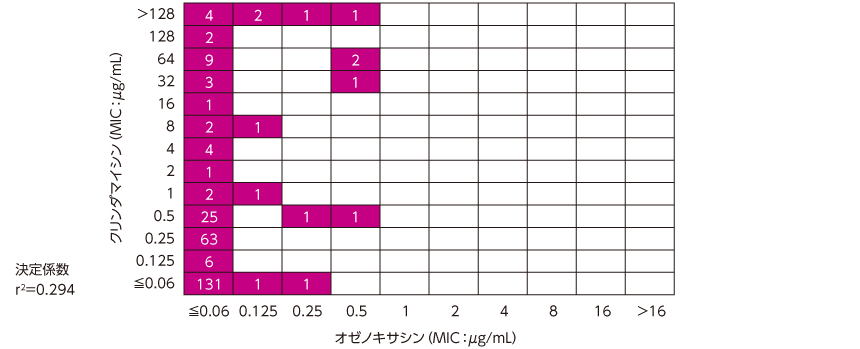
C. acnes の臨床分離株に対するMICの散布図
オゼノキサシンのC. acnes に対するMIC範囲は≦0.06~0.5μg/mLであった。
| 臨床株(分離株数) | 抗菌薬 | MIC範囲(μg/mL) | MIC50(μg/mL) | MIC90(μg/mL) |
|---|---|---|---|---|
| C. acnes(266) | オゼノキサシン | ≦0.06 ~ 0.5 | ≦0.06 | ≦0.06 |
| ナジフロキサシン | ≦0.06 ~ 16 | 0.25 | 0.5 | |
| クリンダマイシン | ≦0.06 ~ >128 | ≦0.06 | 8 | |
| S. aureus(23) | オゼノキサシン | ≦0.06 ~ 0.125 | ≦0.06 | ≦0.06 |
| ナジフロキサシン | ≦0.06 | ≦0.06 | ≦0.06 | |
| クリンダマイシン | 0.125 ~ >128 | 0.125 | >128 | |
| S. epidermidis(229) | オゼノキサシン | ≦0.06 ~ 8 | ≦0.06 | 0.125 |
| ナジフロキサシン | ≦0.06 ~ >128 | ≦0.06 | 2 | |
| クリンダマイシン | ≦0.06 ~ >128 | 0.125 | >128 | |
| Other CNS(82) | オゼノキサシン | ≦0.06 ~ 4 | ≦0.06 | ≦0.06 |
| ナジフロキサシン | ≦0.06 ~ 128 | ≦0.06 | 1 | |
| クリンダマイシン | ≦0.06 ~ >128 | 0.125 | >128 |
MIC50:50%の菌株の発育を阻止する濃度、MIC90:90%の菌株の発育を阻止する濃度
Nakajima A, et al. J Med Microbiol. 65(8), 745(2016)より作表
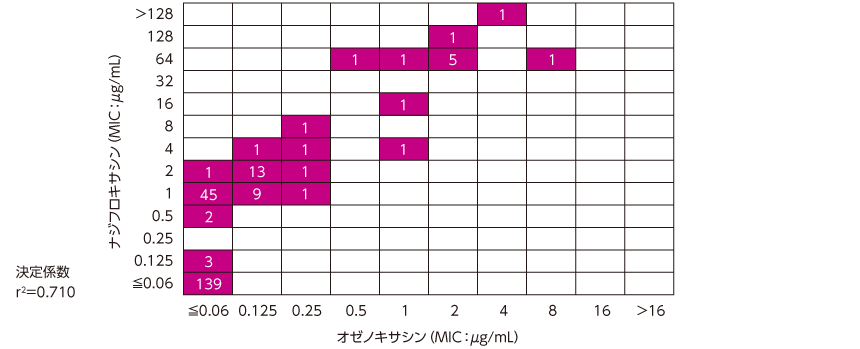
S. epidermidis の臨床分離株に対するMICの散布図
オゼノキサシンのS. epidermidis に対するMIC範囲は≦0.06~8μg/mLであった。
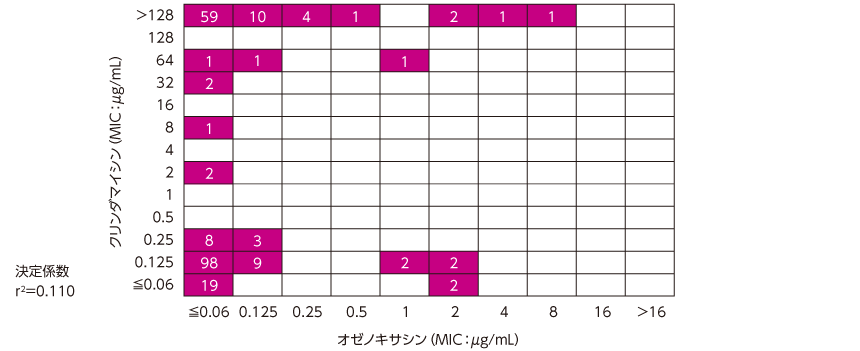
Nakajima A,et al.J med Microbiol.65 (8),745(2016)
〔利益相反 本試験はマルホ株式会社の資金提供により実施された。著者のうち7名がマルホ株式会社社員である。〕
オゼノキサシンの methicillin-susceptible Staphylococcus aureus 及び methicillin-resistant Staphylococcus aureus に対するin vitro 及び in vivo 殺菌作用
表在性皮膚感染症の主要原因菌であるmethicillin-susceptible Staphylococcus aureus(MSSA)及びmethicillin-resistant Staphylococcus aureus(MRSA)に対するオゼノキサシンのin vitro 及びin vivo 殺菌作用について、既存の抗菌薬と比較検討した。
オゼノキサシンの4×MICを曝露したときのtime-kill assayの結果、MSSA株及びMRSA株に対して、経時的に強い殺菌作用を示した。さらに、MSSA株及びMRSA株によるマウス熱傷皮膚感染モデルに対する各抗菌薬塗布による生菌数の減少効果を検討した結果、ゼビアックスローション塗布群は、MSSA株及びMRSA株ともにオゼノキサシンプラセボ塗布群と比較して、有意差が認められた(p<0.01、Tukey test)。
MSSA株及びMRSA株に対するオゼノキサシンの抗菌力 (in vitro )
オゼノキサシンのMSSA臨床分離株 No.28 及び MRSA臨床分離株 No.30 に対する最小発育阻止濃度(MIC)は、それぞれ0.004μg/mL、2μg/mLであった。
| 株 | MIC (μg/mL) | ||||
|---|---|---|---|---|---|
| OZNX | NDFX | LVFX | GM | FA | |
| MSSA臨床分離株 No.28 |
0.004 | 0.03 | 0.25 | 0.5 | 0.25 |
| MRSA臨床分離株 No.30 |
2 | 16 | 512 | 128 | 0.5 |
OZNX:オゼノキサシン、NDFX:ナジフロキサシン、LVFX:レボフロキサシン、GM:ゲンタマイシン、FA:フシジン酸ナトリウム
- 試験方法
-
2012年に表在性皮膚感染症患者より分離されたMSSA 臨床分離株 No.28、MRSA 臨床分離株 No.30に対する各種抗菌薬のMICをCLSI※1に準じた微量液体希釈法により測定した。なお、CLSIの基準に従い、オキサシリンのMICが≦2μg/mLの菌株をMSSA、オキサシリンのMICが≧4μg/mLの菌株をMRSAとした。
※1:Clinical and Laboratory Standards Institute
MSSA株に対するオゼノキサシンの殺菌作用 (in vitro )
オゼノキサシンは、MSSA臨床分離株 No.28に対して、薬剤曝露1時間後より、経時的に強い殺菌作用を示した。
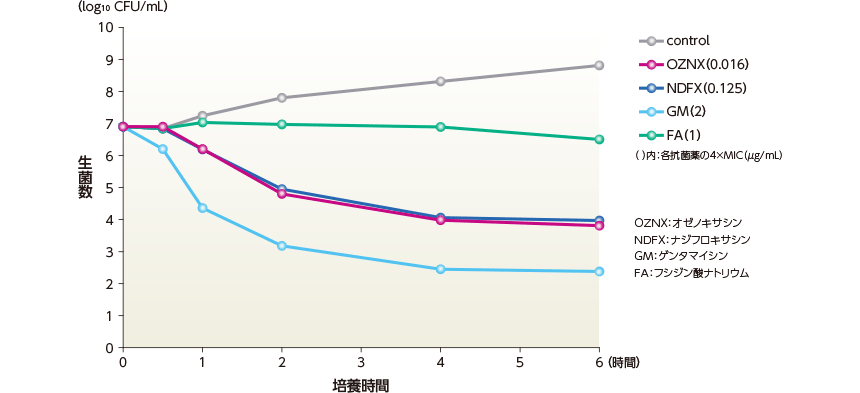
MRSA株に対するオゼノキサシンの殺菌作用 (in vitro )
オゼノキサシンは、MRSA臨床分離株 No.30に対して、薬剤曝露2時間後より、経時的に強い殺菌作用を示した。
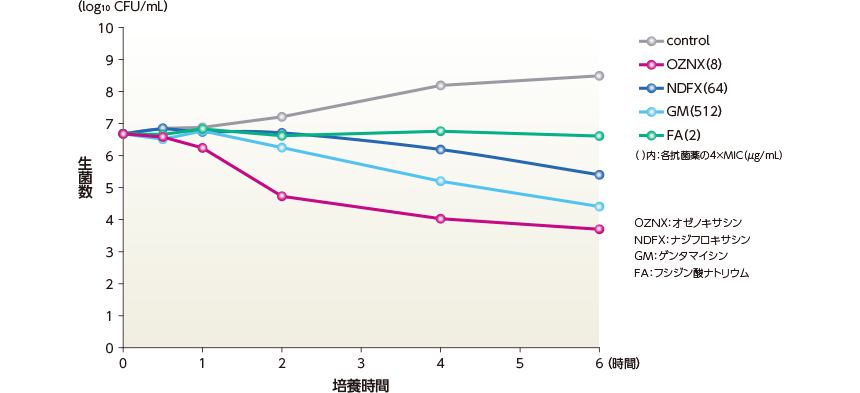
- 試験方法
-
オゼノキサシン、ナジフロキサシン、ゲンタマイシン及びフシジン酸ナトリウム(それぞれ4×MIC)の存在下で35℃で0.5、1、2、4及び6時間培養した。その後、寒天培地に塗抹し、35℃1日間好気条件下で培養後、コロニー数を計測し、生菌数(log10 CFU/mL)を算出した。
MSSA株を用いた熱傷皮膚感染モデルに対するオゼノキサシンの菌数減少効果(マウス)
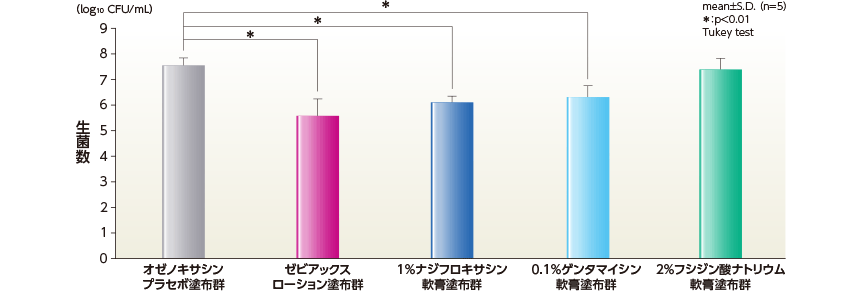
MSSA臨床分離株 No.28によるマウス熱傷皮膚感染モデルにおいて、ゼビアックスローション塗布群、1%ナジフロキサシン軟膏塗布群及び0.1%ゲンタマイシン軟膏塗布群では、薬剤塗布24時間後の感染部位における生菌数に対してオゼノキサシンプラセボ塗布群と比較して、有意差が認められた(p<0.01、Tukey test)。
2%フシジン酸ナトリウム軟膏塗布群では、オゼノキサシンプラセボ塗布群との有意差は認められなかった。
MRSA株を用いた熱傷皮膚感染モデルに対するオゼノキサシンの菌数減少効果(マウス)
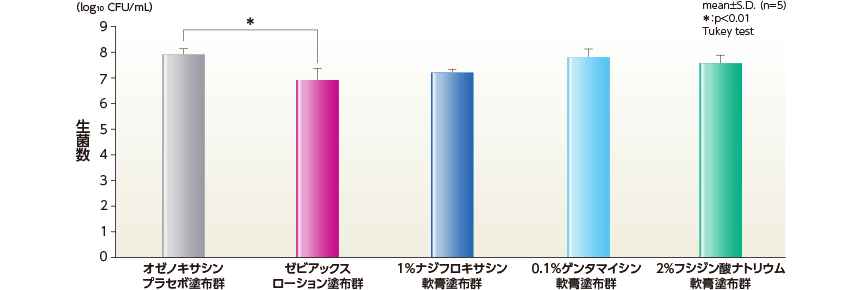
MRSA臨床分離株 No.30によるマウス熱傷皮膚感染モデルにおいて、ゼビアックスローション塗布群は、薬剤塗布24時間後の感染部位における生菌数に対してオゼノキサシンプラセボ塗布群と比較して、有意差が認められた(p<0.01、Tukey test)。
1%ナジフロキサシン軟膏塗布群、0.1%ゲンタマイシン軟膏塗布群及び2%フシジン酸ナトリウム軟膏塗布群では、オゼノキサシンプラセボ塗布群との有意差は認められなかった。
- 試験方法
-
ICR※2系マウス(6週、雄)の背部皮膚を剃毛し、そこに100℃の分銅を10秒間接触させ熱傷を作製し、直後に菌懸濁液を皮内接種した。菌接種24時間後にオゼノキサシンプラセボ、ゼビアックスローション、1%ナジフロキサシン軟膏、0.1%ゲンタマイシン軟膏及び2%フシジン酸ナトリウム軟膏をそれぞれ閉塞経皮投与した。各種抗菌薬投与24時間後に直径2cmの熱傷部位の皮膚を採取し、寒天培地に塗抹し、35℃1日間好気培養後、コロニー数を計測し、生菌数(log10 CFU/mL)を算出した。
※2:Institute of Cancer Research
- 解析方法
- 算出結果はTukey testにて統計処理を行い、オゼノキサシンプラセボ塗布群及び対照抗菌薬塗布群と群間比較した。なお、統計学的有意差をp<0.01とした。
〔利益相反〕本研究に関する費用は、マルホ株式会社が負担した。また、論文の著者にはマルホ株式会社の社員を含む。



