ラピフォートの主要な副作用:眼の調節障害(散瞳、羞明、霧視等)
眼の調節障害(散瞳、羞明、霧視等)は医薬品リスク管理計画書(RMP)にて重要な特定されたリスクに設定しています1)。
ラピフォートの抗コリン作用により、羞明、霧視、散瞳等の眼の調節障害があらわれることがあるので、自動車の運転等、危険を伴う機械の操作に従事する際には注意するよう患者に十分に説明してください2)。
RMP設定理由
ラピフォートは抗コリン作用を有しており、散瞳、羞明、霧視等の眼の調節障害を引き起こすことがあります。血中に移行したラピフォートの有効成分(グリコピロニウム)がこれらの症状を引き起こしている可能性に加え、ラピフォートの剤型(ワイプ剤)の特徴として薬剤が付着した手で眼に触れることにより直接曝露し、眼の調節障害が発現する可能性があります。自動車の運転等の危険を伴う機械の操作中に眼の調節障害が発現した場合、重大な事故につながるおそれがあり、また、散瞳に伴い、特に閉塞隅角緑内障を有する患者では眼圧が上昇し、緑内障の悪化又は急性緑内障発作を発症するおそれがあることから、眼の調節障害を重要な特定されたリスクに設定しています1)。
発現状況
電子添文に記載の発現頻度
羞明、散瞳、霧視(1%以上)2)
視力低下(1%未満)2)
国内臨床試験での発現状況
国内第II/III相試験(M606102-02試験)での副作用発現状況1)
| 副作用名 | ラピフォート群 | プラセボ群 |
|---|---|---|
| 散瞳 | 3.6%(6/168例) | 0.6%(1/165例) |
| 羞明 | 2.4%(4/168例) | 0.6%(1/165例) |
| 霧視 | 1.8%(3/168例) | 1.2%(2/165例) |
国内第Ⅲ相長期投与試験(M606102-03試験)での副作用発現状況1)
| 副作用名 | ラピフォート群 |
|---|---|
| 散瞳 | 2.7%(5/183例) |
| 羞明 | 3.8%(7/183例) |
| 霧視 | 2.7%(5/183例) |
| 視力低下 | 0.5%(1/183例) |
市販後の発現状況
市販後の副作用発現状況は、「市販後副作用件数のご報告」をご参照ください。
発現時期
臨床試験での発現時期
| 有害事象名 | ~4週 | 4週~12週 | 12週~24週 | 24週~36週 | 36週~52週 | 52週~ |
|---|---|---|---|---|---|---|
| 散瞳 | 1例 | 1例 | 2例 | 1例 | 0例 | 0例 |
| 羞明 | 5例 | 1例 | 2例 | 0例 | 0例 | 0例 |
| 霧視 | 2例 | 1例 | 1例 | 1例 | 2例 | 0例 |
| 視力低下 | 0例 | 0例 | 1例 | 0例 | 0例 | 0例 |
市販直後調査における発現時期
市販直後調査*では、眼の調節障害は、55例60件(散瞳29件、羞明23件及び霧視8件)報告され、そのうち、投与開始日又は発現日が不明の40件を除く、20件の発現時期は1日~36日(中央値4.5日)で、65.0%が7日以内に発現しました3)。

部位(両眼/片眼)別の発現状況
臨床試験での部位別発現状況
国内第Ⅲ相長期投与試験(M616102-03試験)で発現した有害事象の部位別発現状況4)
| 有害事象名 | 両眼 | 片眼 |
|---|---|---|
| 散瞳 | 3件 | 8件 |
| 羞明 | 8件 | 4件 |
| 霧視 | 14件 | 2件 |
| 視力低下 | 1件 | 0件 |
市販直後調査における部位別の発現状況
散瞳、羞明は片眼のみの発現例も認められました。片眼での発現例では、本剤使用後の手洗いを失念したことにより副作用が発現したと考えられる症例が認められています。本剤を扱った後は、その手で眼に触れず、直ちに手をよく洗うことをご指導ください3)。
| 副作用名 | 両眼 | 片眼 | 不明 |
|---|---|---|---|
| 散瞳 | 9件 | 13件 | 7件 |
| 羞明 | 9件 | 4件 | 10件 |
| 霧視 | 3件 | 0件 | 5件 |
副作用発現後の投与状況
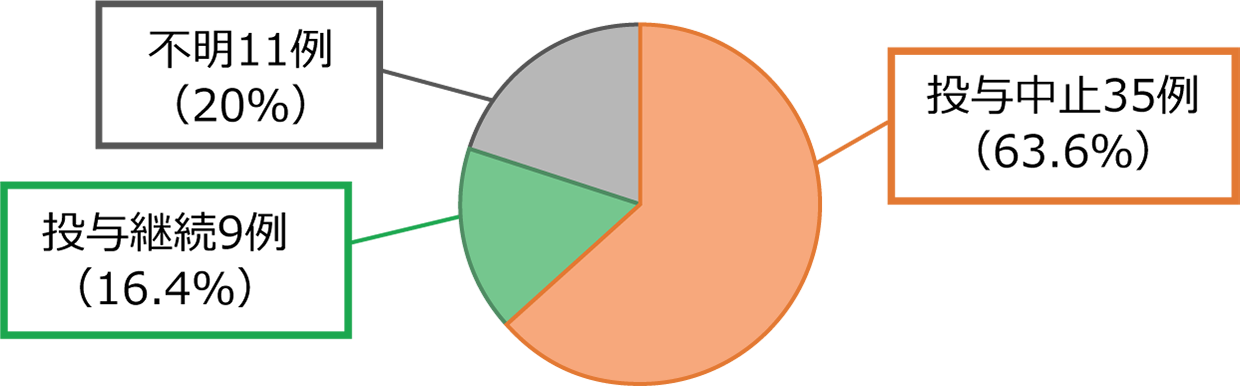
市販直後調査における副作用発現後の投与状況
市販直後調査*では、眼の調節障害発現後、35例では本剤の投与が中止され、9例では本剤の投与が継続されました。なお、複数事象の発現例については、最終の投与状況を示しています3)。
転帰
臨床試験での転帰
国内第Ⅲ相長期投与試験(M616102-03試験)で発現した有害事象の転帰4)
| 有害事象名 | 回復 | 軽快 | その他※ |
|---|---|---|---|
| 散瞳 | 11件 | 0件 | 0件 |
| 羞明 | 13件 | 0件 | 0件 |
| 霧視 | 15件 | 1件 | 0件 |
| 視力低下 | 1件 | 0件 | 0件 |
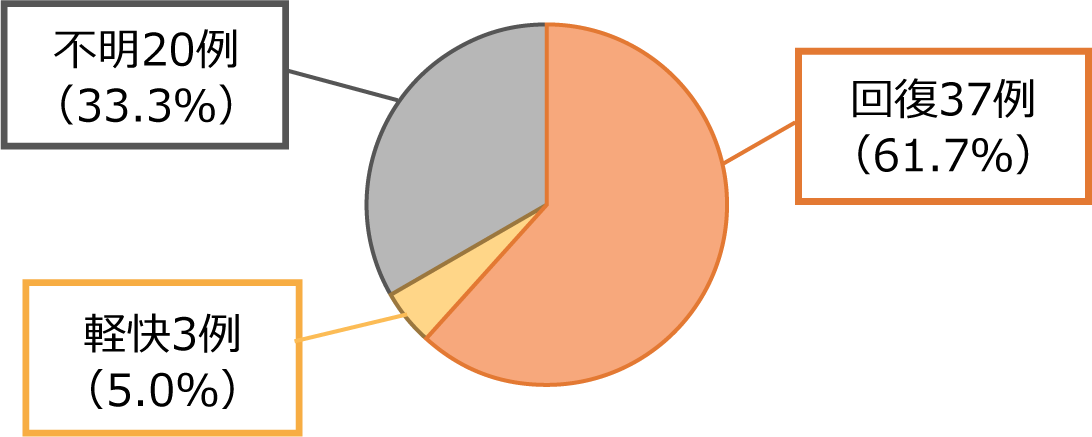
市販直後調査での転帰
市販直後調査*では、眼の調節障害は、転帰不明の20件を除く、40件全件で回復・軽快が確認されました3)。
回復・軽快するまでの期間
臨床試験で発現した有害事象が回復・軽快するまでの期間
| 有害事象名 | 1日 | 2日 | 3日 | 4-7日 | 8-14日 | 15日以上 |
|---|---|---|---|---|---|---|
| 散瞳 | 4件 | 4件 | 0件 | 1件 | 1件 | 1件 |
| 羞明 | 8件 | 1件 | 0件 | 1件 | 1件 | 2件 |
| 霧視 | 10件 | 3件 | 0件 | 0件 | 2件 | 0件 |
| 視力低下 | 0件 | 0件 | 0件 | 0件 | 0件 | 1件 |
市販直後調査における回復・軽快するまでの期間
市販直後調査*では、眼の調節障害発現後、回復・軽快に至った40件のうち発現日及び転帰日が報告された18件では、発現から回復・軽快するまでの期間は1日~44日(中央値3日)で、3件を除き7日以内に回復・軽快しました。回復・軽快までの期間が44日の1件は、薬局来院時に回復を確認されたものであり、実際に症状が消失した日は不明です3)。

対処法
ラピフォート投与後は、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行ってください。
ラピフォートの薬液が眼に入った場合、羞明、霧視等の眼の調節障害があらわれることがあります。また、刺激を感じることがあるので、眼に入らないよう注意してください。万一、眼に入った場合は、直ちに水で洗い流してください2)。
電子添文の記載
- 2. 禁忌(次の患者には投与しないこと)
-
- 2.1
- 閉塞隅角緑内障の患者[抗コリン作用により眼圧が上昇し、症状を悪化させることがある。]
- 8. 重要な基本的注意
-
- 8.1
- 抗コリン作用により、羞明、霧視、散瞳等の眼の調節障害があらわれることがあるので、自動車の運転等、危険を伴う機械の操作に従事する際には注意するよう患者に十分に説明すること。
- 11. 副作用
- 次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には使用を中止するなど適切な処置を行うこと。
- 11.2 その他の副作用
- 羞明、散瞳、霧視(1%以上)、視力低下(1%未満)
- 14. 適用上の注意
- 14.1 薬剤交付時の注意
-
- 14.1.3
- 本剤を扱った後は、その手で眼に触れず、直ちに手をよく洗うこと。
- 14.1.4
- 本剤の薬液が眼に入った場合、羞明、霧視等の眼の調節障害があらわれることがある。また、刺激を感じることがあるので、眼に入らないよう注意すること。万一、眼に入った場合は、直ちに水で洗い流すこと。
参考資料
- ラピフォートワイプ2.5%に係る医薬品リスク管理計画書
- ラピフォートワイプ2.5%電子添文
- ラピフォートワイプ2.5%市販直後調査*の結果報告(2022年5月23日~2022年11月22日)
- 申請資料概要(ラピフォートワイプ2.5%に関する資料)



