太田母斑、扁平母斑、異所性蒙古斑、外傷性色素沈着症に対する皮膚レーザー照射療法時の疼痛緩和(第Ⅲ相比較臨床試験)
試験概要
試験デザイン
多施設共同プラセボ対照無作為化二重盲検並行群間比較試験
対象
15歳以上の太田母斑、扁平母斑、異所性蒙古斑及び外傷性色素沈着症患者
方法
試験薬非貼付部位にレーザーを6ショット照射しVASを評価した後、ペンレステープまたはプラセボ1~6枚を60分間貼付し、除去後、レーザーの照射エネルギーを変えずに6ショット照射しVASを評価した。
有効性および安全性解析対象
ペンレステープ群 58例、プラセボ群 30例
評価項目
主要評価項目:VAS変化率=(非貼付部位のVAS値-貼付部位のVAS値)×100/非貼付部位のVAS値
※VAS(Visual Analogue Scale):100mmのスケールを用い、痛みを評価する視覚アナログスケール。数値が大きい方が痛みは強い。
副次評価項目:試験薬貼付部位のVAS値、VAS変化量、試験薬貼付部位のVRS値
安全性:有害事象、バイタルサインの推移、臨床検査値の推移
解析計画
主要評価項目のVAS変化率の群間比較は2標本t検定を用いた。有意水準はすべて両側5%とした。
VAS変化率(主要評価項目)
VAS変化率の平均±標準偏差は、ペンレステープ群は-26.71±41.69%、プラセボ群は-6.74±35.08%であり、ペンレステープ群はプラセボテープ群に対して有意な差が認められた。
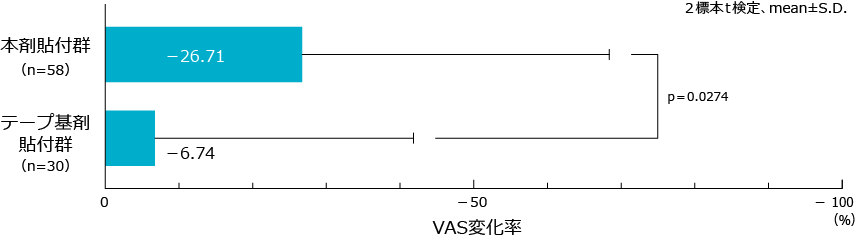
*1:VAS(Visual Analogue Scale):100mmのスケールを用い痛みを評価する視覚アナログスケール。数値が大きい方が痛みは強い。
*2:VAS変化率:(非貼付部位のVAS値-貼付部位のVAS値)×100/非貼付部位のVAS値
本試験における副作用
ペンレステープ群において、適用部位紅斑が58例中3例(5.2%)および蕁麻疹が58例中1例(1.7%)に、プラセボ群において適用部位紅斑が30例中1例(3.3%)に認められた。
- 用法・用量に関する使用上の注意(一部抜粋)
- 皮膚レーザー照射療法時の疼痛緩和に使用する場合、小児における本剤の貼付枚数は、体重、患部の大きさを考慮して、必要最小限にとどめること(「小児等への投与」、「臨床成績」の項参照)。
著者のうち2名はマルホ株式会社の社員である。



