適正使用情報4:ヘマンジオル初回投与時及び増量時の確認事項
適正使用のために必要な医療連携を適宜行ってください。
【重要な基本的注意】の確認
【重要な基本的注意】(抜粋)
(1)初回投与時及び増量時は、小児科医との連携のもと、心拍数、血圧、呼吸状態、血糖値等を少なくとも投与2時間後まで1時間毎に確認すること。
増量方法
添付文書では、本剤の初回投与時及び増量時の入院管理、外来管理の区分は規定されていません。
初回投与時及び増量時のバイタルサイン等の管理においては、小児科医との連携のもとで行うようにしてください。
参考:専門医による治療ガイダンス
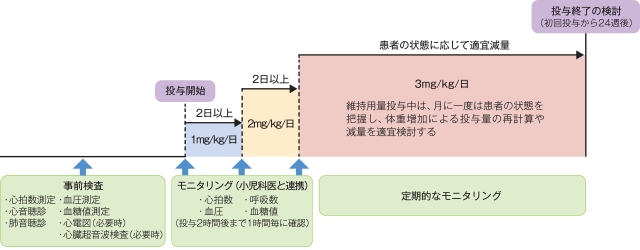
入院管理での実施
生命又は機能を脅かすおそれのある合併症を伴う場合には、入院管理の下、3mg/kg/日(分2)まで増量するのが望ましい。増量は2日以上の間隔をあける。
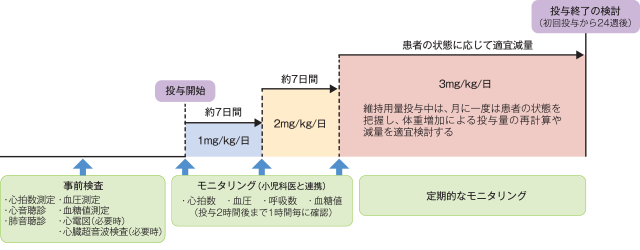
外来管理での実施
生命又は機能を脅かすおそれのある合併症がなければ、外来管理の下、3mg/kg/日(分2)まで増量することも可能である。受診の時期(7日程度)に合わせて増量するのが望ましい。
投与継続の必要性の検討
【重要な基本的注意】(抜粋)
(6)本剤による治療にあたっては経過を十分観察し、投与開始24週間を目安に有効性を評価し、本剤による治療継続の必要性を検討すること。
<参考>
① 国内第Ⅲ相臨床試験での24週投与後の追跡調査(36週まで)1)
〈3mg/kg/日 24週間投与〉
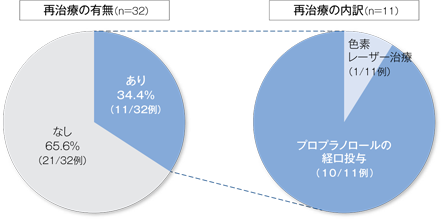
再治療の有無
追跡調査を完了した32例において、24週から36週後までの追跡調査期間に乳児血管腫の再治療が必要であった割合は34.4%(11/32例)であった。10例は他のプロプラノロール製剤による再治療で、1例は色素レーザー治療であった。
② 海外第Ⅱ/Ⅲ相臨床試験での24週投与後の追跡調査(96週まで)2)
〈3mg/kg/日 24週間投与〉
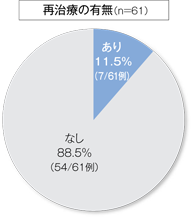
再治療の有無
24週後に有効と判定され追跡調査に移行した症例61例において、24週から96週後の追跡調査期間に乳児血管腫の再治療が必要であった割合は11.5%(7/61例)であった。
- 乳児血管腫患者を対象とした第Ⅲ相臨床試験(承認時評価資料)
- 乳児血管腫患者を対象とした第Ⅱ/Ⅲ相臨床試験(承認時評価資料)



