コムクロシャンプーの臨床試験(頭部の尋常性乾癬)
頭部の尋常性乾癬患者を対象とした第Ⅲ相臨床試験1,2)
試験概要
- 目的
- 頭部に尋常性乾癬の皮疹を有する患者を対象に、コムクロシャンプーの有効性及び安全性を、コムクロシャンプープラセボ(以下、プラセボ)を対照とした二重盲検並行群間比較試験により検討する。
- 対象
- 尋常性乾癬患者
- 選択基準
-
治療開始日に以下の条件を満たす患者
- 頭部面積に対する頭部の尋常性乾癬の病変面積の割合が30%以上
- PSSI(Psoriasis Scalp Severity Index)皮疹重症度合計スコアが6以上
- GSS(Global Severity Score)が「中等度」以上
- 年齢が16歳以上(同意取得日に満たす必要あり)
- 症例数
- 有効性解析集団FAS(Full Analysis Set:最大の解析対象集団)
157例(コムクロシャンプー群78例、プラセボ群79例) - 投与方法
- コムクロシャンプー又はプラセボを、乾燥した頭部に患部を中心に適量を1日1回(4週間)塗布し、15分後に水又は湯で泡立てて洗い流した。
- 評価項目
-
有効性
主要評価項目:4週後のPSSI 75達成率
副次評価項目:
- 4週後のGSSが「消失」又は「ほぼ消失」と判定された患者の割合
- 4週後のPSSIスコア
- 4週後のPSSIスコア減少率
- 4週後のNRS(Numerical Rating Scale)
- 4週後のDLQI(Dermatology Life Quality Index)スコア変化量
その他の評価項目:
- 各評価日のPSSI 50達成率
- 各評価日のPSSI 75達成率
- 4週後のPSSI皮疹重症度合計スコア
- 4週後の各皮膚所見の重症度スコア など
利便性患者評価(患者アンケート調査)
頭皮乾癬の症状の煩わしさについて
コムクロシャンプーについて など安全性
有害事象(自覚症状及び他覚所見、臨床検査値異常変動)及び臨床検査値
- 解析計画
-
主要評価項目
4週後のPSSI 75達成率の解析では、有意水準を両側5%、信頼係数を両側95%とした。FASを対象に群別に達成率を算出し、連続修正を伴ったピアソンのカイ二乗検定を行った。また、両群間の差の推定値と信頼区間を算出した。
副次評価項目
FASを対象に解析を行い、検定の際は複数項目間及び群間の多重性の調整は行わず、一律に有意水準は両側5%とし、信頼係数も一律両側95%とした。
- 4週後のGSSが「消失」又は「ほぼ消失」と判定(治療成功)された患者の割合:群別に割合を算出し、連続修正を伴ったピアソンのカイ二乗検定を行った。また、両群間の差について推定値及び信頼区間を算出した。
- 4週後のPSSIスコア:各評価時期のPSSIスコアを応答変数とした反復測定分散分析を行い、対比によって4週後のPSSIスコアに対する両群間の検定を行った。また、最小二乗推定値とその信頼区間を算出した。
- 4週後のPSSIスコア減少率:各評価時期のPSSIスコア減少率を応答変数、治療開始日のPSSIスコアを共変量とした反復測定分散分析を行い、対比によって4週後のPSSIスコア減少率に対する両群間の検定を行った。また、最小二乗推定値とその信頼区間を算出した。なお、算出の際には群全体における共変量の平均値を用いた。
- 4週後のNRS:2)と同様の解析を行った。
- 4週後のDLQIスコア変化量:治療開始日及び4週後(中止症例は中止来院日)のDLQIについて、群ごとに総合得点と六つの下位尺度別の要約統計量を算出した。また、治療開始日から4週後(中止症例は中止来院日)の変化量に対して、群別に総合得点と六つの下位尺度別の要約統計量を算出した。
その他の評価項目
FASを対象に解析を行い、一律に有意水準は両側5%とし、信頼係数も一律両側95%とした。
- 各評価日のPSSI 50達成率:投与群別に各評価日の達成率を算出し、連続修正を伴ったピアソンのカイ二乗検定を行った。
- 各評価日のPSSI 75達成率:1)と同様の解析を行った。
- 4週後のPSSI皮疹重症度合計スコア:各評価時期のPSSI皮疹重症度合計スコアを応答変数とした反復測定分散分析を行い、対比によって4週後のPSSI皮疹重症度合計スコアに対する両群間の検定を行った。また、最小二乗推定値とその信頼区間を算出した。
- 4週後の各皮膚所見の重症度スコア:3)と同様の解析を行った。
利便性患者評価(患者アンケート調査)
質問別に治療開始日及び4週後/中止来院日の回答の頻度と割合を算出した。
試験デザイン
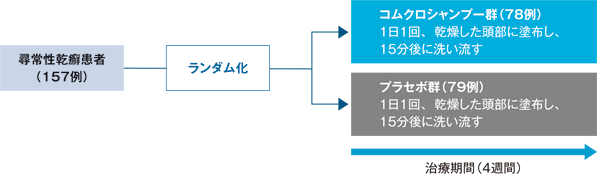
有効性
PSSIスコア
4週後のPSSI 75達成率(FAS)[主要評価項目]
4週後のPSSI 75達成率(PSSIスコア減少率が75%以上の割合)は、コムクロシャンプー群では29.5%(23/78例)、プラセボ群では7.6%(6/79例)であり、両群間で統計学的に有意な差が認められた(P<0.001、連続修正を伴ったピアソンのカイニ乗検定)。
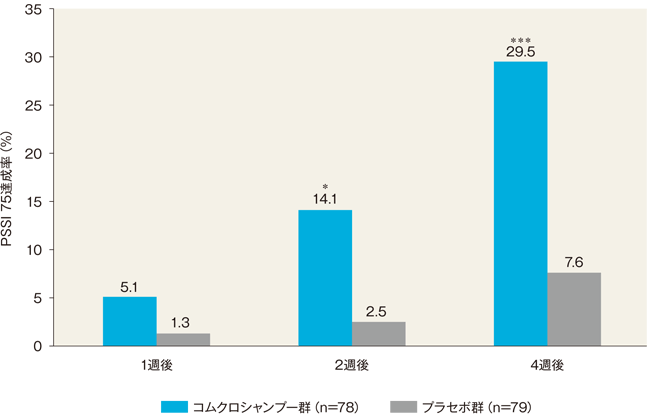
*:P<0.05、***:P<0.001、連続修正を伴ったピアソンのカイニ乗検定(vs プラセボ群)
各評価日のPSSI 50達成率(FAS)[その他の評価項目]
2、4週後のPSSI 50達成率(PSSIスコア減少率が50%以上の割合)は、それぞれコムクロシャンプー群では34.6%(27/78例)、57.7%(45/78例)、プラセボ群では12.7%(10/79例)、22.8%(18/79例)であり、いずれも両群間で統計学的に有意な差が認められた(P<0.01、P<0.001、連続修正を伴ったピアソンのカイニ乗検定)。
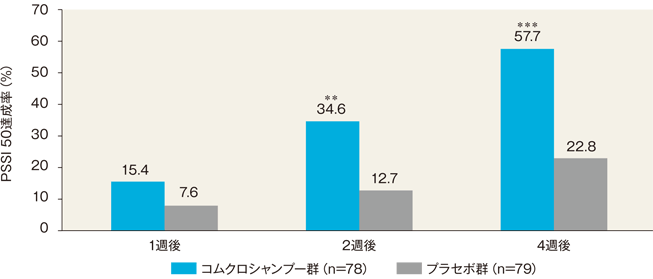
**:P<0.01、***:P<0.001、連続修正を伴ったピアソンのカイニ乗検定(vs プラセボ群)
4週後のPSSIスコア(FAS)[副次評価項目]
4週後のPSSIスコア(最小二乗平均値)は、コムクロシャンプー群では16.3、プラセボ群では25.1であった。両群間の差(コムクロシャンプー群-プラセボ群)は−8.9(95%信頼区間:−12.5~−5.2)であり、統計学的に有意な差が認められた(P<0.001、反復測定分散分析)。
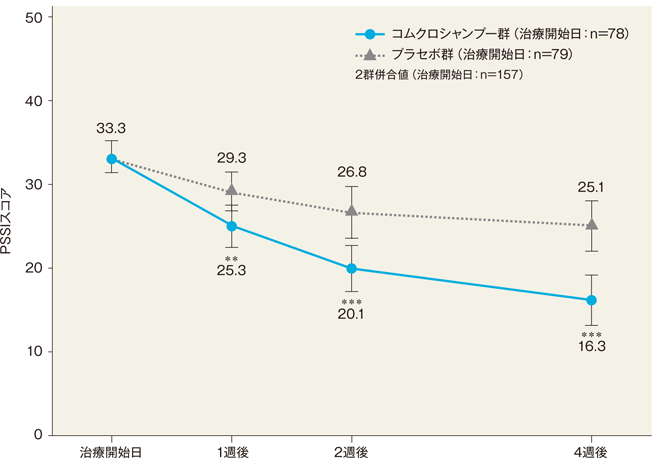
最小二乗平均値±95%信頼区間
**:P<0.01、***:P<0.001、反復測定分散分析(vs プラセボ群)
4週後のPSSIスコア減少率(FAS)[副次評価項目]
4週後のPSSIスコア減少率(最小二乗平均値)は、コムクロシャンプー群では52.3%、プラセボ群では23.7%であった。両群間の差(コムクロシャンプー群-プラセボ群)は28.6%(95%信頼区間:17.2%~40.0%)であり、統計学的に有意な差が認められた(P<0.001、反復測定分散分析)。
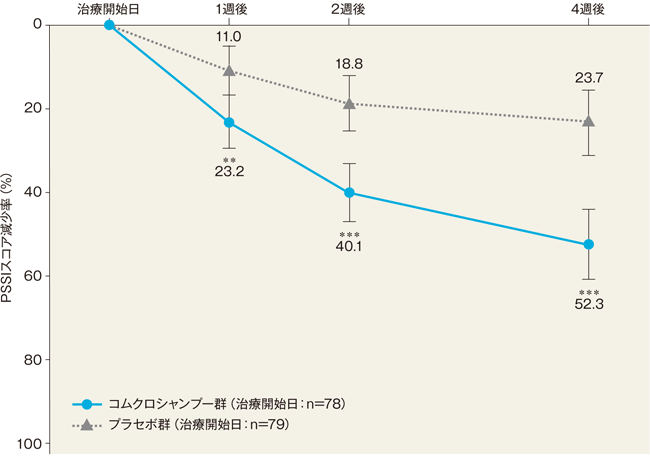
最小二乗平均値±95%信頼区間
**:P<0.01、***:P<0.001、反復測定分散分析(vs プラセボ群)
4週後のPSSI皮疹重症度合計スコア(FAS)[その他の評価項目]
4週後のPSSI皮疹重症度合計スコア(最小二乗平均値)は、コムクロシャンプー群では4.3、プラセボ群では6.0であった。両群間の差(コムクロシャンプー群-プラセボ群)は−1.7(95%信頼区間: −2.4~−1.0)であり、統計学的に有意な差が認められた(P<0.001、反復測定分散分析)。
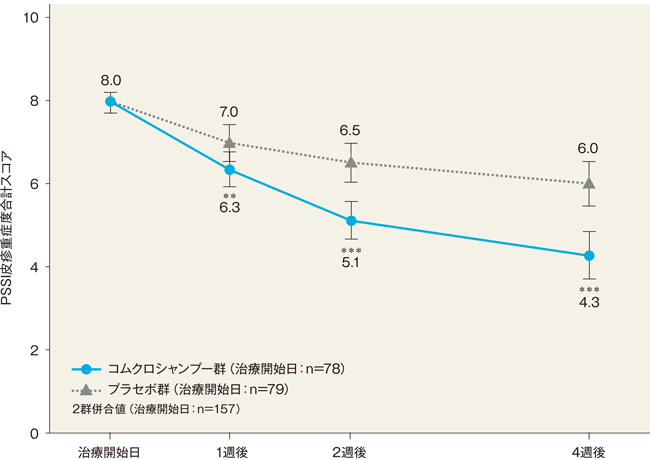
最小二乗平均値±95%信頼区間
**:P<0.01、***:P<0.001、反復測定分散分析(vs プラセボ群)
4週後の各皮膚所見の重症度スコア(FAS)[その他の評価項目]
4週後の紅斑、浸潤/肥厚及び鱗屑の重症度スコア(最小二乗平均値)は、コムクロシャンプー群では1.7、1.3及び1.3、プラセボ群では2.1、1.9及び2.0であった。両群間の差(コムクロシャンプー群-プラセボ群)はそれぞれ、−0.4、−0.6及び−0.7(95%信頼区間:−0.7~−0.2、−0.9~−0.4及び−1.0~−0.4)であり、統計学的に有意な差が認められた(いずれもP<0.001、反復測定分散分析)。
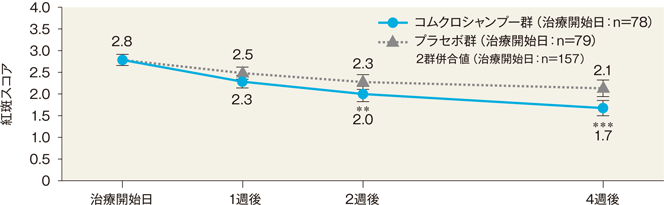
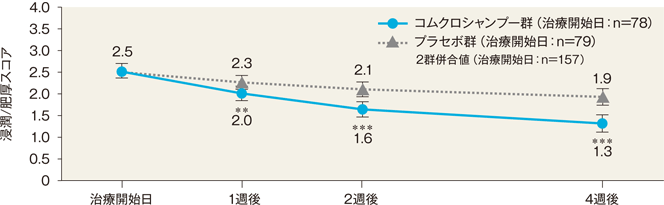
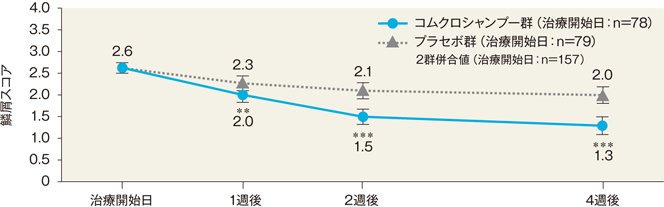
最小二乗平均値±95%信頼区間
**:P<0.01、***:P<0.001、反復測定分散分析(vs プラセボ群)
判定基準:PSSI(Psoriasis Scalp Severity Index)
PSSIスコアとは、尋常性乾癬(頭部)の主な症状である紅斑、浸潤/肥厚、鱗屑の各皮膚所見を独立して評価するとともに、病変範囲も評価可能な指標である3)。頭部における各皮膚所見(紅斑、浸潤/肥厚、鱗屑)の重症度、及び頭部面積に対する頭部の尋常性乾癬の病変面積(%)をスコア化し、これらを計算式に当てはめてPSSIスコアを算出した。
<PSSI皮疹重症度合計スコア計算式> PSSI皮疹重症度合計スコア=紅斑スコア+浸潤/肥厚スコア+鱗屑スコア (最大で12点)
<PSSIスコア計算式> PSSIスコア=(紅斑スコア+浸潤/肥厚スコア+鱗屑スコア)×病変範囲スコア (最大で72点)
| PSSIスコア減少率 | = | (治療開始日のPSSIスコアー評価日のPSSIスコア)×100 |
| 治療開始日のPSSIスコア |
| スコア | 各皮膚所見(紅斑、浸潤/肥厚、鱗屑)重症度 |
|---|---|
| 0点 | なし |
| 0.5点 | なしと軽度の中間 |
| 1点 | 軽度 |
| 1.5点 | 軽度と中等度の中間 |
| 2点 | 中等度 |
| 2.5点 | 中等度と高度の中間 |
| 3点 | 高度 |
| 3.5点 | 高度と極めて高度の中間 |
| 4点 | 極めて高度 |
| スコア | 頭部面積に対する頭部の 尋常性乾癬の病変面積 |
|---|---|
| 0点 | 0% |
| 1点 | 0% < ~ < 10% |
| 2点 | 10% ≦ ~ < 30% |
| 3点 | 30% ≦ ~ < 50% |
| 4点 | 50% ≦ ~ < 70% |
| 5点 | 70% ≦ ~ < 90% |
| 6点 | 90% ≦ ~ ≦ 100% |
- Thaçi, D., et al.: Dermatology, 203(2), 153(2001)
GSS
4週後のGSSが「消失」又は「ほぼ消失」と判定された患者の割合(FAS)[副次評価項目]
4週後のGSSが「消失」又は「ほぼ消失」と判定(治療成功)された患者の割合は、コムクロシャンプー群では11.5%(9/78例)、プラセボ群では2.5%(2/79例)であり、両群間で統計学的に有意な差は認められなかった(P=0.058、連続修正を伴ったピアソンのカイニ乗検定)。
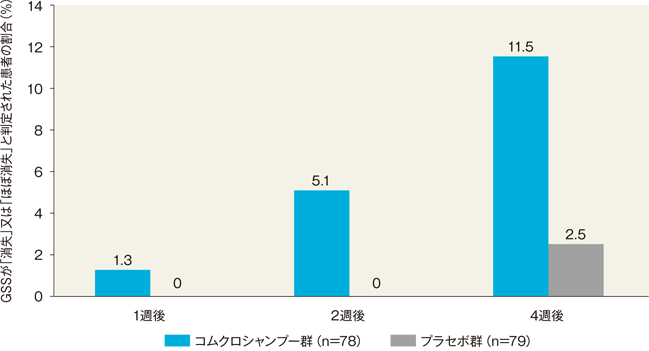
連続修正を伴ったピアソンのカイニ乗検定(VS プラセボ群)
判定基準:GSS(Global Severity Score:全般重症度)
GSSとは、頭部の紅斑、浸潤/肥厚、鱗屑の特徴から疾患の重症度を判定するための指標であり、「消失」、「ほぼ消失」、「軽度」、「中等度」、「重度」、「極めて重度」の6段階で総合的に判定する。GSSが「消失」又は「ほぼ消失」と判定された患者の割合を「治療成功」とした。
| 重症度 | 定義 |
|---|---|
| 消失 | 臨床的な所見、症状はなし。 |
| ほぼ消失 | 非常にわずかな所見、症状がみられる。(非常に細かい鱗屑や、わずかな紅斑がみられる。) |
| 軽度 | わずかな所見、症状がみられる。(軽度の紅斑、鱗屑を伴う皮疹がみられ、いくつかの皮疹は隆起していることがかろうじて分かる。) |
| 中等度 | 中等度の所見、症状がはっきりみられる。(明瞭な紅斑と鱗屑を伴う皮疹がみられ、しばしば正常皮膚より盛り上がっている。) |
| 重度 | 重度の所見、症状がみられる。(強い紅斑、多くの鱗屑がこぼれおちる境界明瞭な、厚く肥厚した皮疹が全体的に最も頻繁にみられる。) |
| 極めて重度 | 非常に重度の所見、症状がみられる。(最大限にまで赤くなった紅斑、大量の鱗屑、顕著に盛り上がった皮疹がみられる。深刻な場合、膿疱もみられる。) |
NRS
参考情報
4週後のNRS(FAS)[副次評価項目]
4週後のNRS(最小二乗平均値)は、コムクロシャンプー群では2.4、プラセボ群では4.0であった。両群間の差(コムクロシャンプー群-プラセボ群)は−1.6(95%信頼区間:−2.3~−1.0)であり、統計学的に有意な差が認められた(P<0.001、反復測定分散分析)。
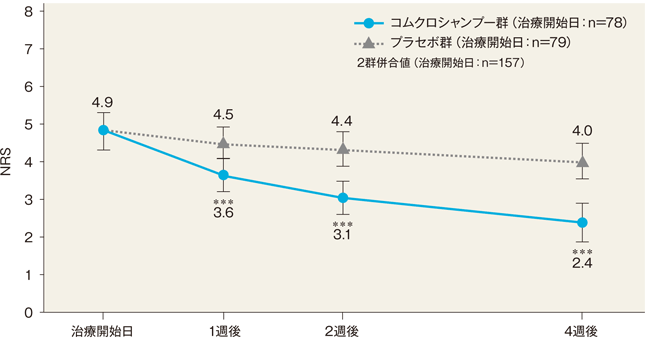
最小二乗平均値±95%信頼区間
***:P<0.001、反復測定分散分析(vs プラセボ群)
判定基準:NRS(Numerical Rating Scale)
NRSとは、そう痒の評価項目として用いられている指標である。患者自身が各来院日直前24時間の平均的なそう痒の状態を、0を「かゆみなし」、10を「最大のかゆみ(頭部の尋常性乾癬により過去に経験した最大のかゆみ)」として11段階で回答することで評価した。
QOL
4週後のDLQIスコア変化量(FAS)[副次評価項目]
治療開始日及び4週後/中止来院日のDLQIスコア(平均値)は、コムクロシャンプー群では5.6及び2.3、プラセボ群では5.9及び5.1であった。
DLQI合計スコアのカテゴリが1段階以上改善した患者は、コムクロシャンプー群では60.3%(47/78例)、プラセボ群では32.9%(26/79例)であった。
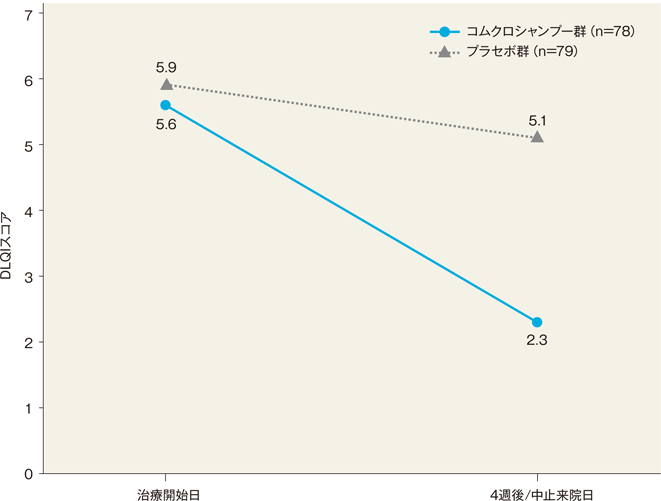
判定基準:DLQI(Dermatology Life Quality Index)
DLQIは皮膚疾患のためのQOL尺度4)であり、症状・感情、日常活動、レジャー、仕事・学校、人間関係及び治療の6つの下位尺度から構成されている。様々な皮膚疾患のQOL評価として用いられている。なお、本試験では、DLQIを頭部の尋常性乾癬に限定し、改変して使用している。
| DLQI合計スコア | 皮膚関連QOLの総合的影響度 |
|---|---|
| 0~1 | 全く影響がない |
| 2~5 | 少し影響がある |
| 6~10 | 中程度の影響がある |
| 11~20 | 大きな影響がある |
| 21~30 | 非常に影響がある |
- Finlay, AY., et al.: Clin Exp Dermatol, 19(3), 210(1994)
利便性患者評価(患者アンケート調査)
頭皮乾癬の症状の煩わしさについて
- 対 象:
- 全症例157例(コムクロシャンプー群78例、プラセボ群79例)
- 調査時期:
- 治療開始日
- 調査方法:
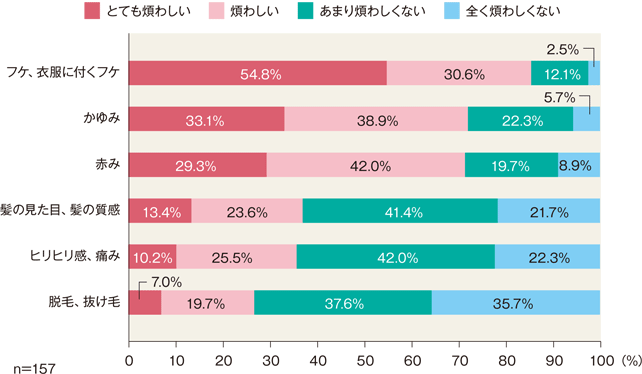
- フケ、かゆみ、赤み等の頭皮症状について「とても煩わしい」、「煩わしい」、「あまり煩わしくない」、「全く煩わしくない」で回答する。
治療開始日に頭皮乾癬の各症状で「とても煩わしい」又は「煩わしい」と回答した患者の割合は、「フケ、衣服に付くフケ」が85.4%(134/157例)、「かゆみ」が72.0%(113/157例)、「赤み」が71.3%(112/157例)、「髪の見た目、髪の質感」が36.9%(58/157例)、「ヒリヒリ感、痛み」が35.7%(56/157例)、「脱毛、抜け毛」が26.8%(42/157例)であった。
コムクロシャンプーについて
参考情報
- 対 象:
- コムクロシャンプー群78例
- 調査時期:
- 4週後/中止来院日
- 調査方法:
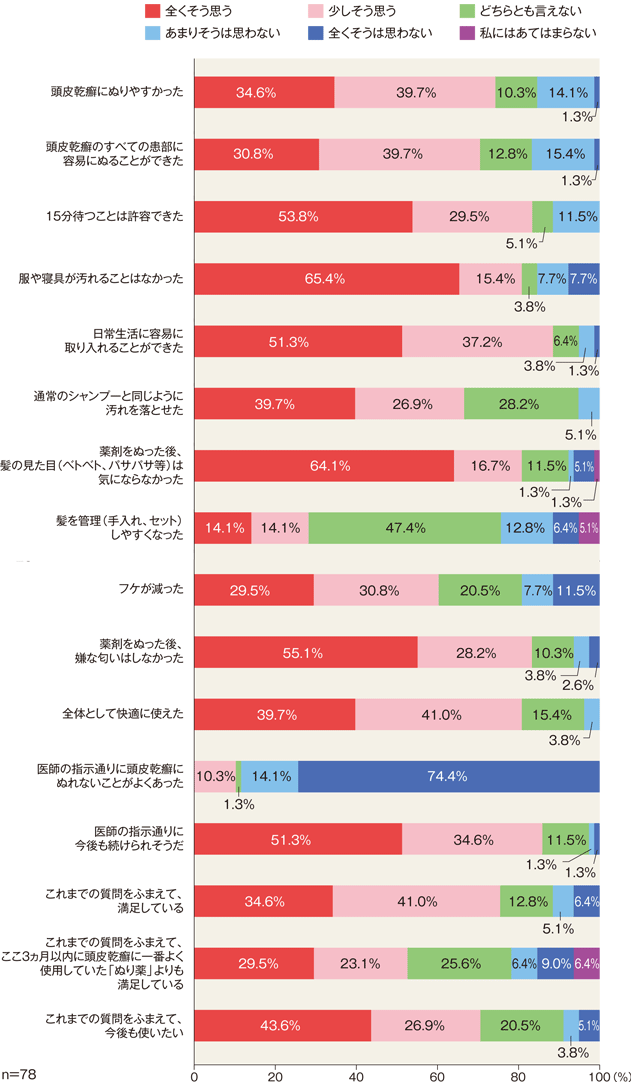
- コムクロシャンプーの塗りやすさ、使用感、治療満足度等について「全くそう思う」、「少しそう思う」、「どちらとも言えない」、「あまりそうは思わない」、「全くそうは思わない」、「私にはあてはまらない」で回答する。
4週後/中止来院日に実施した利便性患者評価では、コムクロシャンプーについて「全くそう思う」又は「少しそう思う」と回答した患者の割合は、「頭皮乾癬にぬりやすかった」が74.4%(58/78例)、「15分待つことは許容できた」が83.3%(65/78例)、「日常生活に容易に取り入れることができた」が88.5%(69/78例)、「これまでの質問をふまえて、満足している」が75.6%(59/78例)であった。
安全性
本試験において、副作用は、コムクロシャンプー群78例中には認められなかった。
| コムクロシャンプー群 | プラセボ群 | |
|---|---|---|
| 安全性解析対象例数 | 78 | 79 |
| 副作用発現例数(%) | 0 | 2(2.5) |
| 副作用の種類 | 副作用発現例数(%) | |
|---|---|---|
| コムクロシャンプー群 | プラセボ群 | |
| 皮膚および皮下組織障害 | 0 | 1(1.3) |
| 皮膚炎 | 0 | 1(1.3) |
| 一般・全身障害および投与部位の状態 | 0 | 1(1.3) |
| 適用部位刺激感 | 0 | 1(1.3) |
- 7. 用法・用量に関連する注意
- 本剤使用中には患者の病態を十分観察し、使用4週間を目安に本剤の必要性を検討し、漫然と使用を継続しないこと。
[17.1.1-17.1.3参照]
- 8.1
- 本剤の使用により症状の改善がみられない場合又は症状の悪化をみる場合は使用を中止すること。
- 8.2
- 眼及び眼瞼皮膚へ付着した場合、白内障、緑内障を含む眼障害が発現する可能性がある。眼及び眼瞼皮膚へ付着しないよう注意し、付着した場合は直ちに水で洗い流すこと。
- 頭皮の尋常性乾癬患者を対象とした第Ⅲ相臨床試験(プラセボ対照試験)(承認時評価資料)
- Nakagawa, H., et al.: 臨床医薬, 33(2), 163(2017) [利益相反]本試験に関する費用はマルホ株式会社が負担した。著者のうち3名はマルホ株式会社の社員である。著者にはマルホ株式会社より講演料、コンサルタント料などを受領している者が含まれる。



